Produkt wurde in den Korb gelegt
Sie haben 0 Artikel in Ihrem Warenkorb. Es gibt 1 Artikel in Ihrem Warenkorb.

ECOPOSTURAL stellt mit Hilfe des IBV Instituts sein Therapieliegensortiment auf das neue Medizinproduktegesetz (MDR) ein.
Das Inkrafttreten der neuen europäischen Verordnung über das neue Medizinprodukt (MDR) bedeutete eine kleine Revolution in der Branche, die von den Unternehmen einige Anstrengungen erforderte, sich an diese neuen Rahmenbedingungen anzupassen. Das Institut für Biomechanik (IBV) berät Unternehmen im GESUNDHEITS-Sektor, wie ECOPOSTURAL, ein führendes Unternehmen im Bereich Gesundheitsmöbel, mit erteilter Herstellungserlaubnis seit 2000 von der AEMPS (Staatliche Agentur für Arzneimittel und Gesundheitsprodukte), setzen auf Qualität und Sicherheit ihrer Medizinprodukte als Elemente der Markenidentifikation setzen.
ZIELSETZUNG
Ziel der Zusammenarbeit mit dem Institut für Biomechanik (IBV) und der Firma ECOPOSTURAL ist die gemeinsame Erarbeitung der in den technischen Unterlagen (Technical File) enthaltenen Dokumentation wie von der neuen Medizinprodukteverordnung zur Beschreibung und Einstufung des Produkts bis hin zur Begründung und Erklärung des Designs und des Herstellungsprozesses. Bei dieser Gelegenheit, die klinische Bewertung, die Risikoanalyse und das Post-Marketing-System für seine Therapieliegen. Dafür hat das IBV dem Unternehmen sein gesamtes Wissen zur Zertifizierung, Entwicklung und Bewertung von Medizinprodukten der Klassen I, IIa, IIb und III zur Verfügung gestellt.
EINLEITUNG
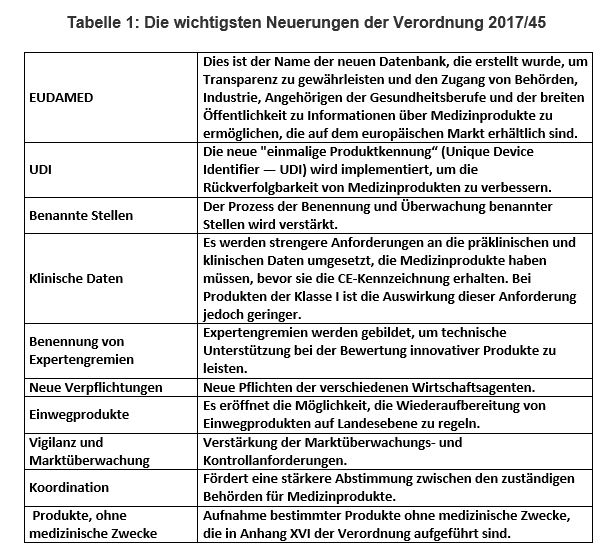
Am 26. Mai 2021 trat die neue Medizinprodukteverordnung (EU) 2017/745 (MDR) in der EU - Europäischen Union in Kraft, als Ergebnis der Arbeiten der Mitgliedstaaten und der Europäischen Kommission in Zusammenarbeit mit den an Medizinprodukten beteiligten Branchen. Diese, am 5. April 2017, veröffentlichte Verordnung ändert die Richtlinie 2001/83/EG, die Verordnung (EG) Nr. 178/2002 und die Verordnung (EG) Nr. 1223/2009 und hebt die Richtlinien 90/385/EWG und 93/42/ EWG des Rates. Ziel dieser Verordnung ist es, die Verfügbarkeit wirksamer, hochwertiger und sicherer Medizinprodukte auf dem Markt zu gewährleisten. Zu den wichtigsten Neuerungen, die einführt werden, gehört eine Verbesserung der Rückverfolgbarkeit von Produkten, die Schaffung einer großen Datenbank als Garantie für Transparenz oder die Forderung nach strengeren Anforderungen an präklinische und klinische Daten. Die Tabelle 1 präsentiert die herausragendsten Neuerungen gegenüber der früheren europäische Medizinprodukterichtlinie 93/42/EWG. .
WACHSTUM
Innerhalb der Zusammenarbeit des IBV mit der Firma ECOPOSTURAL bei der Erstellung der Dokumentation, die in den technischen Unterlagen enthalten ist, wurde das gesamte Sortiment an Liegen des Unternehmens analysiert und nach ähnlichen Merkmalen und Vorteilen gruppiert. Für jede der Gruppen wurde eine Risikoanalyse durchgeführt und ihre angemessene Behandlung begründet. Die kontinuierliche Anforderung an Eigenschaften der Materialien und Komponenten von Zweitlieferanten, die von ECOPOSTURAL seit seiner Gründung umgesetzt werden, und die Vorbereitung von Tests gemäß den Vorschriften durch das IBV sind Aspekte, die Risiken reduzieren und die höchste Qualität des Produkts sicherstellen. Die ECOPOSTURAL-Liegen wurden in den IBV-Labors nach Testverfahren getestet, die an die Norm UNE-EN 60601-2-52:2010/A1:2015, Elektromedizinische Geräte, angepasst sind. Teil 2-52: Besondere Anforderungen an die grundlegende Sicherheit und die wesentlichen Leistungsmerkmale von Krankenhausliegen. Die Abbildungen 1, 2 und 3 zeigen die durchgeführten Tests.



Nachdem die Risikoanalysen durchgeführt, die Anforderungen an die Materialien und die Ergebnisse der Bewertungen untersucht wurden, ist der gesamte Prozess korrekt identifiziert und in den technischen Unterlagen dokumentiert, mit der das Unternehmen seine Produkte angemessen zertifizieren kann.
SCHLUSSFOLGERUNGEN
Durch die gemeinsame, auf die Bedürfnisse des Unternehmens zugeschnittene Arbeit des Instituts für Biomechanik (IBV) und ECOPOSTURAL, konnte die Einhaltung der Anforderungen der neuen europäischen Medizinprodukteverordnung sichergestellt werden. Ausserdem hat es die Korrektur und Verbesserung einiger spezifischer Elemente auf Grundlage der Testergebnisse ermöglicht. Als Experte für die Entwicklung und Bewertung von Medizinprodukten berät das IBV das Unternehmen hinsichtlich der Verbesserungen, die es in das Produkt einbringen muss. Daher wird das IBV zu einem Zentrum, das mit Unternehmen der Branche bei der Verbesserung ihrer Produkte zusammenarbeitet und nicht nur deren Gutachter ist. Das vom IBV mit ECOPOSTURAL entwickelte Projekt macht die Notwendigkeit von Technologiezentren in dem valencianischen Gebiet deutlich, wo Unternehmen aus dem Bereich GESUNDHEIT bei dem neuen und komplexen Prozess der Entwicklung, Bewertung und Zertifizierung von Medizinprodukten gemäß der neuen Verordnung (MDR) unterstützt werden.